
Struktur Atom dan Tabel Periodik Unsur Apa itu Struktur Atom dan Tabel Periodik Unsur? MejaKita
E. Menangkap 3 elektron. Soal nomor 19. Atom berikut ini yang mencapai kestabilan dengan mengikuti kaidah duplet adalah.. A. Litium. B. Natrium. C. Magnesium. D. Aluminium. E. Klor. Soal nomor 20. Unsur Y mempunyai konfigurasi elektron 2, 8, 2. Unsur ini lebih mudah membentuk ikatan ion dengan unsur lain yang mempunyai konfigurasi elektron.

Unsur yang paling mudah menangkap elektron adalah unsur.
Ikatan kimia adalah gaya yang mengikat atom-atom atau ion-ion dalam suatu molekul atau senyawa. Konsep tentang ikatan kimia pertama kali dikemukakan pada tahun 1916 oleh Gilbert Newton Lewis dari Amerika dan Albrecht Kossel dari Jerman.Penemuan konsep tentang ikatan kimia ini didasari dari beberapa kenyataan tentang sifat-sifat atom dalam unsur yaitu sebagai berikut:
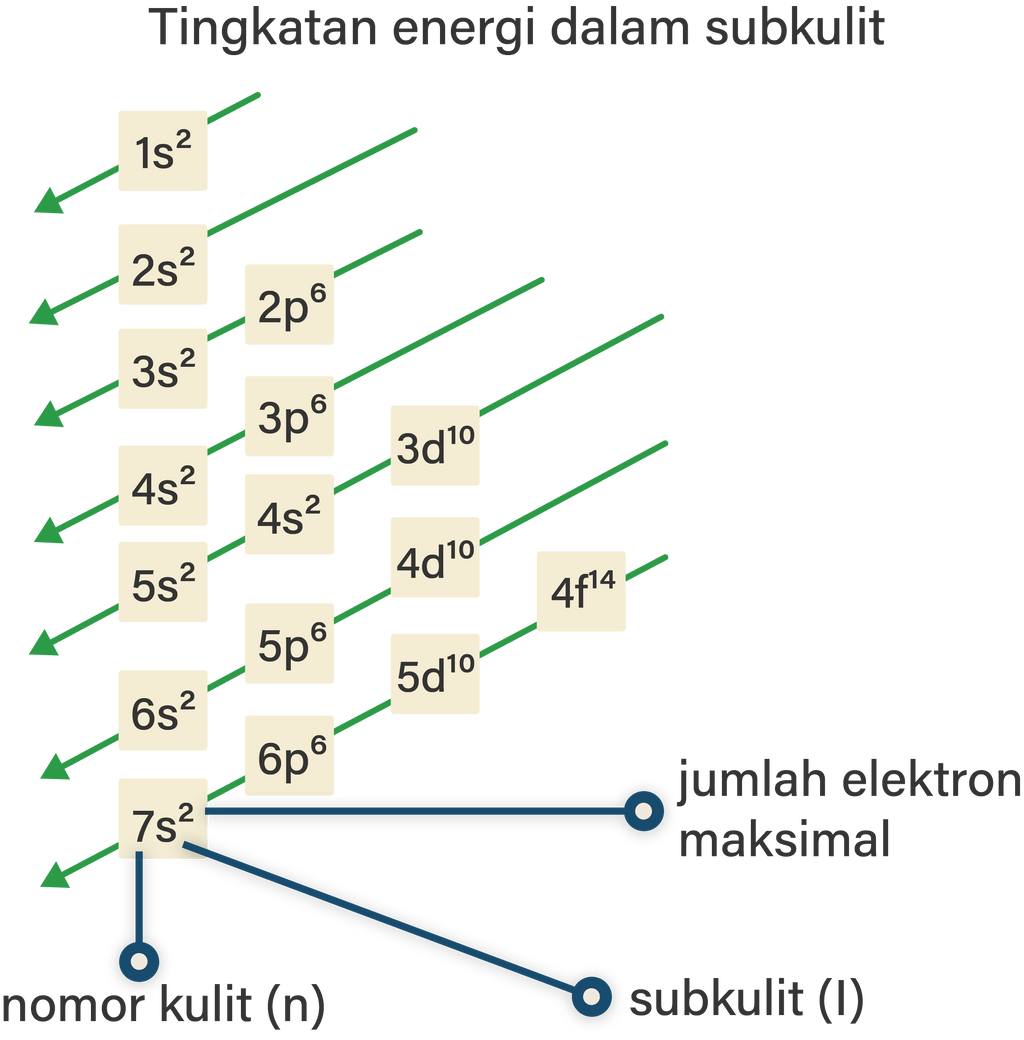
Jelaskan tentang konfigurasi elektron beserta cont...
17 Cl = 1s 2 2s 2 2p 6 3s 2 3p 5 → 7 elektron di kulit terluar cenderung menangkap 1 elektron lain untuk mencapai kestabilan. Reaksi penangkapan elektron: Cl + e → Cl - Reaksi ikatan ion: Ca 2+ + 2 Cl - → CaCl 2. Jadi, rumus ikatan ion yang terjadi antara unsur Ca dan Cl adalah CaCl 2. Jawaban: E. Itulah pembahasan Quipper Blog kali.

Jumlah elektron valensi dan golongan unsur berikut adalah...
Dibaca Normal 1 menit. Berikut ini penjelasan soal bagaimana proses pembentukan ion, pembentukan senyawa ion, dan contoh senyawa ion. tirto.id - Materi yang ada di dunia ini mengandung partikel-partikel kecil yang tersusun atas atom, ion, beserta molekul. Ion dikenal sebagai atom bermuatan listrik. Banyak zat yang tersusun oleh partikel ion.

Di antara unsur dengan konfigurasi elektron berikut yang
Unsur yang Cenderung Menangkap Elektron: Pahami Sifat Kimia yang Mempengaruhi. Dalam kimia, unsur-unsur dapat memiliki kecenderungan untuk menangkap elektron dalam berbagai situasi, terutama ketika mereka membentuk ikatan kimia dengan unsur lain. Sifat-sifat kimia ini sangat penting dalam memahami reaktivitas unsur-unsur dalam berbagai senyawa.

Unsur berikut ini yang cenderung menangkap elektron adala...
Afinitas elektron adalah besarnya energi yang dilepaskan atau dihasilkan oleh atom pada keadaan gas untuk menangkap satu elektron. Dalam satu golongan dari atas ke bawah, afinitas elektron cenderung makin kecil. Jika unsur mudah menangkap elektron, unsur tersebut memiliki afinitas elektron yang besar. Unsur F, Cl, Br, I, dan At merupakan unsur.
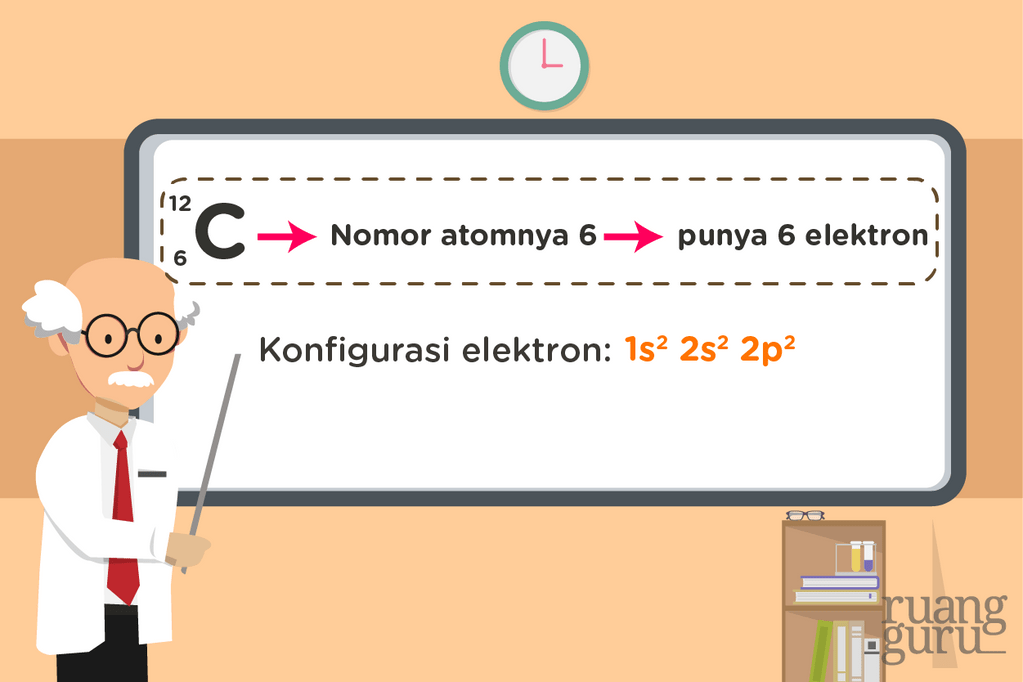
Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
Ada tiga jenis ikatan Kimia, yaitu ikatan kovalen, ikatan logam dan ikatan ion. Sementara itu, dalam membentuk ion, suatu atom akan melepas atau mengikat elektron. Atom-atom yang mempunyai energi ionisasi rendah, misalnya atom-atom dari unsur golongan IA dan IIA dalam sistem periodik unsur akan mempunyai kecenderungan untuk melepaskan elektronnya.

Konfigurasi Elektron
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Unsur berikut ini yang c.

Suatu unsur memiliki notasi 52 24Cr. Diagram orbital yang...
Kelelektronegatifan adalah kecenderungan suatu atom untuk menangkap elektron dan membentuk ion negatif . Di dalam sistem keperiodikan unsur, Kelektronegatifan memiliki sifat sebagai berikut: Pada satu periode, Kelektronegatifan cenderung bertambah dari kiri ke kanan. Pada satu golongan, Kelektronegatifan cenderung berkurang dari atas sampai bawah.

Unsur X Dan Y Mempunyai Konfigurasi Elektron Sebagai Berikut Unsur Unsur
Contoh Soal Kestabilan Unsur dan Pembahasannya. Jelaskan bagaimana terbentuknya ikatan pada senyawa CaCl2 CaCl 2! Pembahasan. Kita tuliskan konfigurasi elektron untuk kedua unsur yang terlibat dalam ikatan. 20Ca 20 Ca: 2, 8, 8, 2. 17Cl 17 Cl: 2, 8, 7. Kalsium (Ca) akan cenderung melepas 2 elektron untuk mencapai kestabilan, membentuk ion (atom.
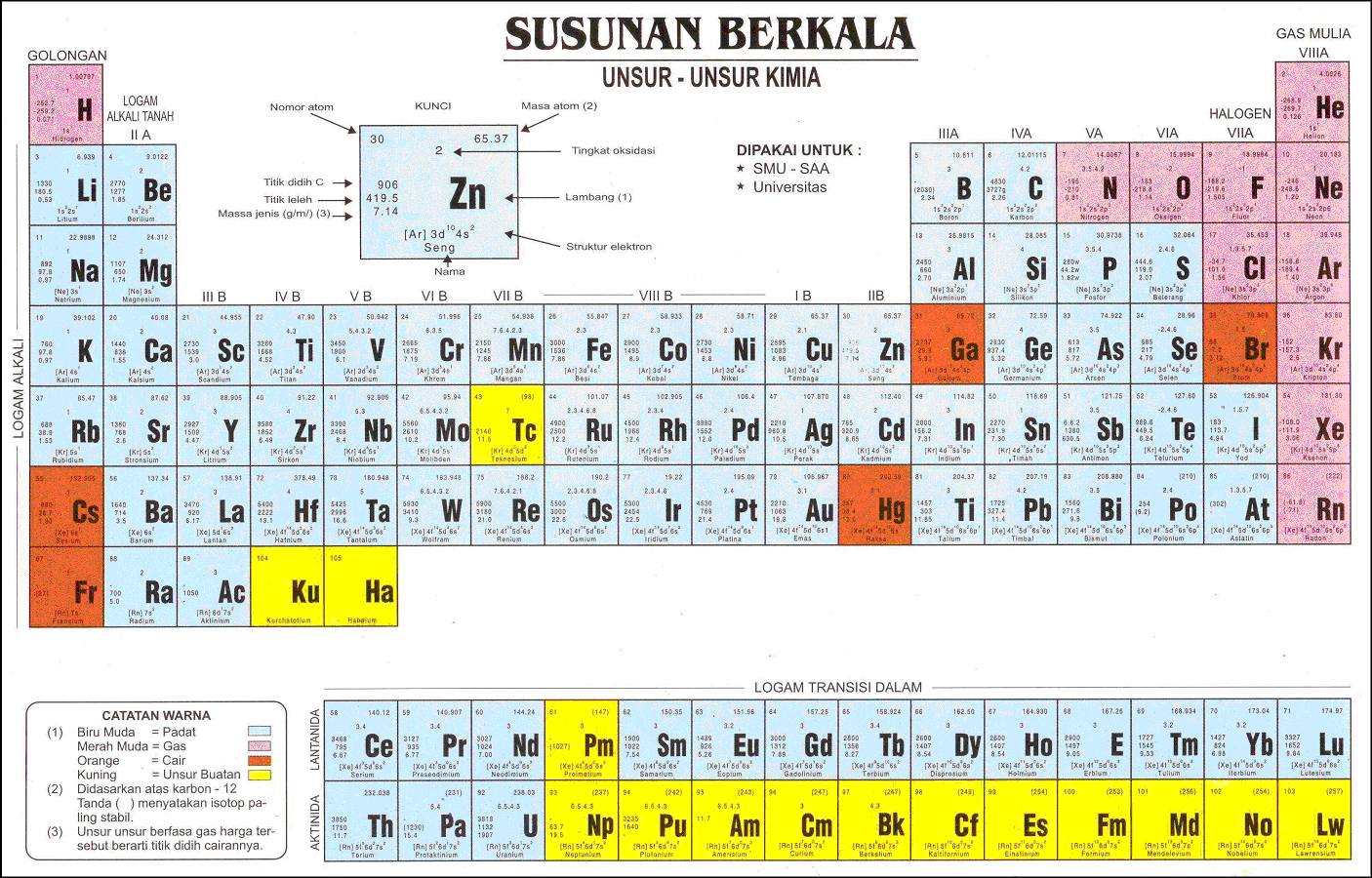
Unsur Kimia Homecare24
Unsur berikut ini yang cenderung menangkap elektron adalah A. 11 Na B. 12 Mg C. 13 Al D. 16 S E. 18 Ar 11. Diketahui unsur-unsur 7 N, 8 O, 9 F, 10 Ne, 11 Na, 12 Mg, 16 S, 19 K, dan 20 Ca. Pasangan di bawah ini yang mempunyai elektron valensi sama adalah.. A. K + dengan Ca 2+ B. Mg 2+ dengan S 2-
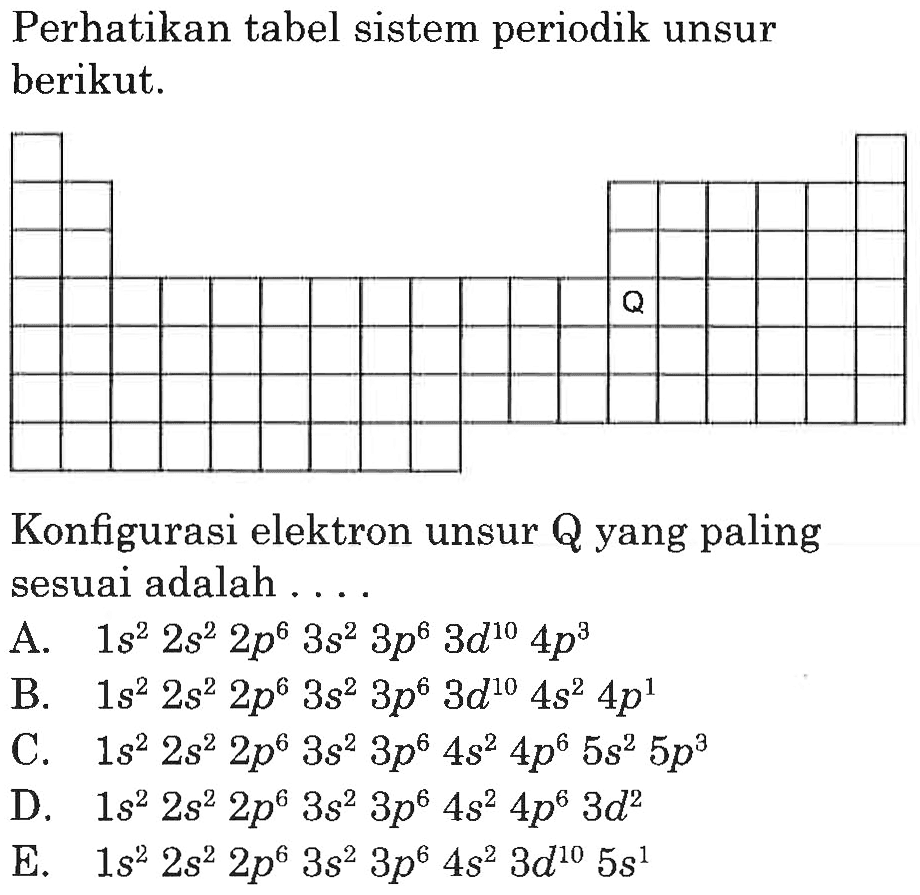
Konfigurasi elektron ion L^(3+) adalah 1s^2 2s^2 2p^6 3s^...
Contoh reaksi yang akan dibahas adalah sebabagi berikut: Pengantar Belajar Kimia Organik 49 Methanol di sisi lain merupakan nukleo l yang buruk apa

Trik Super Kilat Memahami Keelektronegatifan
Lego Friends di sini ada pertanyaan tentang unsur yang cenderung menangkap elektron unsur dari golongan 1A sampai 8A akan mencapai kestabilan dengan cara berikatan dengan unsur lain sesuai dengan kaidah oktet untuk mencapai kestabilan gas mulia yaitu dengan 8 elektron pada kulit terluar golongan 1A sampai golongan 3 akan memiliki kecenderungan untuk melepas elektron golongan 4A memiliki.

Konfigurasi elektron suatu unsur X adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d5. Unsur
Penangkapan elektron atau tangkapan elektron ( penangkapan elektron-K, juga penangkapan-K, atau penangkapan elektron-L, pengangkapan-L) adalah proses ketika inti atom netral yang kaya proton menyerap elektron dari kulit dalam atom, biasanya dari kelopak elektron K atau L. Oleh karena itu, proses ini mengubah proton menjadi neutron dan secara.

Kecenderungan Afinitas Elektron, Penyimpangan, dan Argumennya Urip dot Info
Ikatan ion merupakan ikatan yang terjadi akibat adanya perpindahan elektron yang berasal dari satu atom ke atom lainnya.. Agar dapat memahami mengenai sifat ikatan tersebut, berikut adalah penjelasan dari sifat-sifat ikatan ion.. Kemampuan untuk dapat menghantarkan listrik tersebut karena pada ikatan ion mengandung unsur yang bermuatan.

Konfigurasi Elektron Yang Paling Stabil Adalah cara menghemat air
Sifat Sifat Periodik Unsur. Sifat sifat unsur yang berulang secara periodik disebut pula sifat periodik unsur, yang meliputi: 1. Jari-jari atom dan ion. Jari-jari atom dan ion adalah jarak dari inti atom dengan orbital elektron terluar yang stabil. Jari-jari atom dalam satu golongan dari atas ke bawah cenderung semakin besar karena jumlah kulit.