
Polar and Nonpolar Molecules
2. Ikatan Kovalen Non Polar. Ikatan kovalen nonpolar adalah ikatan kovalen yang terbentuk ketika atom membagikan elektronnya secara setara (sama). Biasanya terjadi ketika ada atom mempunyai afinitas elektron yang sama atau hampir sama. Semakin dekat nilai afinitas elektron, maka semakin kuat ikatannya.

Senyawa Polar Dan Non Polar Pengertian, Ciri, Sifat, Contoh PDF
Polar dan nonpolar lebih merujuk pada ikatan kovalen. Penentuan polaritas ikatan kovalen dapat menggunakan cara numerik, yaitu menghitung perbedaan elektronegativitas atom yang saling berikatan. Pada skala Pauling, jika hasilnya adalah antara 0,4 dan 1,7 secara umum akan disebut sebagai ikatan kovalen polar. Demikian penjelasan mengenai polar.
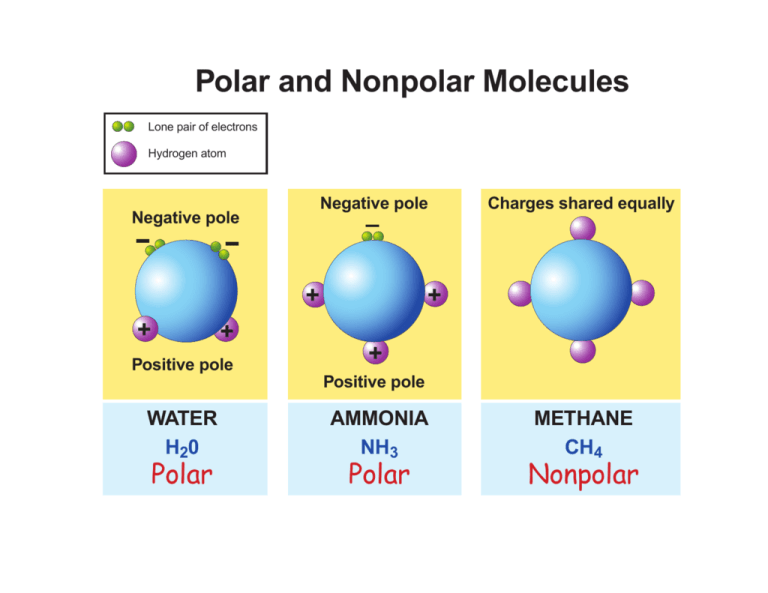
Polar and Nonpolar Molecules
Ikatan Kovalen Nonpolar, Polar dan Koordinasi. a. Ikatan kovalen nonpolar. Nah, bila dua buah atom atau unsur yang terikat dalam ikatan kovalen memiliki keelektronegatifan yang sama besar, maka tidak akan mengakibatkan pengutuban atau polarisasi muatan. Hal ini kemudian dinamakan sebagain ikatan kovalen nonpolar. Misalnya pada I 2 dimana.

perbedaan senyawa ion dan kovalen polar dan non polar Boris Newman
Polar dan non polar adalah konsep dalam kimia yang menggambarkan sifat molekul dalam hal muatan listrik dan kemampuan bersifat polar atau tidak polar. Dalam kehidupan sehari-hari, konsep ini penting untuk memahami interaksi antara zat-zat dan bagaimana reaksi kimia terjadi. Temukan penjelasan lengkap tentang pengertian polar dan non polar di artikel ini.

Ikatan Kimia (8) Cara Menentukan Molekul Polar dan Non Polar Kimia Kelas 10 YouTube
Salah satu bentuk interaksi polar yang umum adalah ikatan hiadrogen, yang juga dikenal sebagai ikatan-H. Misalnya, air membentuk ikatan H dan memiliki massa molar M = 18 dan titik didih +100 °C, dibandingkan dengan nonpolar metana dengan M = 16 dan titik didih -161 °C. Molekul nonpolar. Dalam molekul boron trifluorida, penataan trigonal.

Ikatan Kovalen Polar Dan Nonpolar Beserta Contoh Ikatannya Rumus Kimia Sexiz Pix
B. Pengertian Ikatan Kovalen Polar dan Nonpolar. Ikatan kovalen polar adalah ikatan kovalen yang terbentuk antara atom-atom yang memiliki perbedaan elektronegativitas. Contoh ikatan kovalen polar adalah senyawa HF. Atom H memiliki elektronegativitas 2,20. dan atom F memiliki elektronegativitas 3,98. Artinya terdapat perbedaan elektronegativitas.

Contoh Pelarut Polar Dan Nonpolar Gudang Materi Online
Ciri - Ciri Senyawa Polar. Ada beberapa ciri-ciri senyawa polar yang diantaranya yaitu: Dapat larut dalam air dan pelarut polar lain. Memiliki kutub + dan kutub - akibat tidak meratanya distribusi elektron. Memiliki pasangan elektron bebas "apabila bentuk molekul diketahui" atau memiliki perbedaan keelektronegatifan.
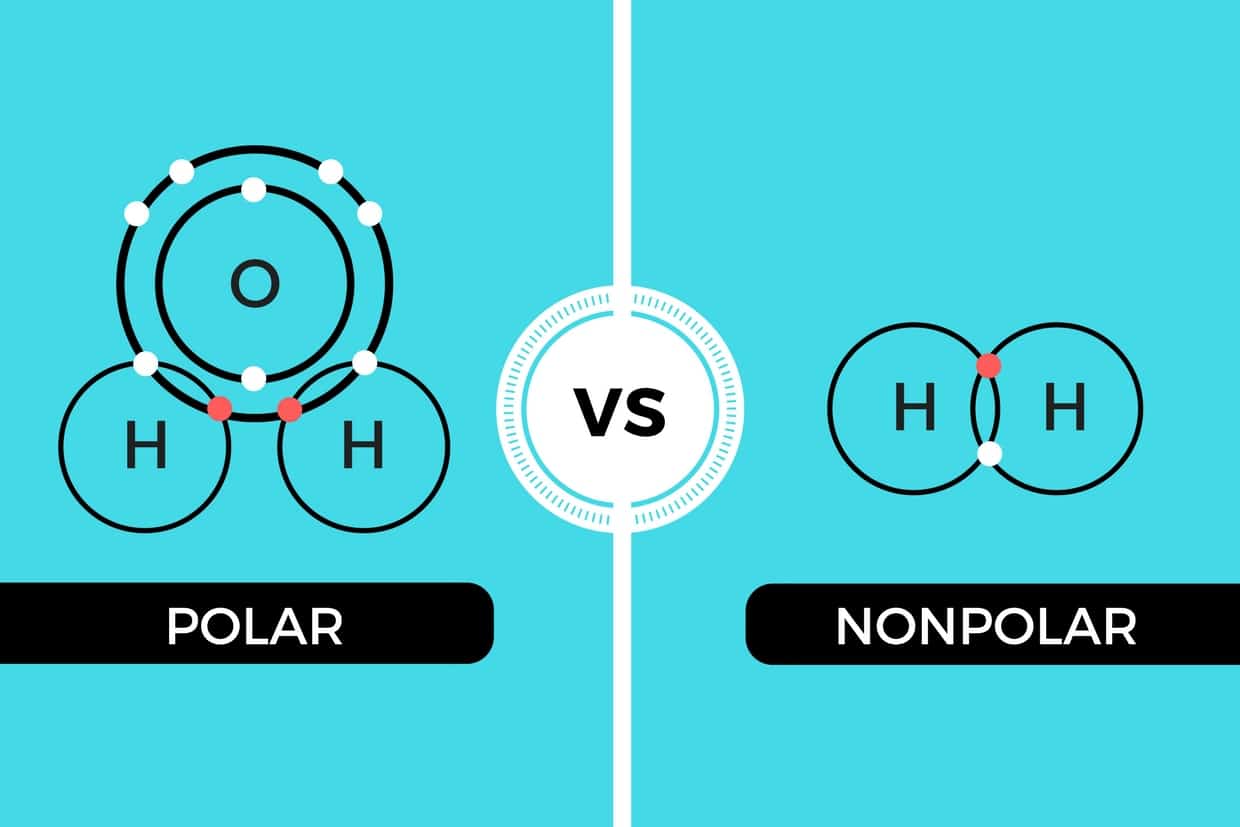
Polar and Nonpolar Covalent Bonds Characteristics & Differences Still Education
Jadi, tetap semangat dan teruslah belajar. Baik kita langsung ke topik. Dari beberapa sumber yang saya dapatkan mengenai kapasitor polar dan nonpolar ini, saya dapati penjelasan mengenai kapasitor polar dan nonpolar sebagai berikut ini. Pengertian Kapasitor Polar dan Nonpolar. 1. Kapasitor Polar. Kapasitor polar adalah jenis kapasitor.

Difference between polar and nonpolar examples
Kalau ikatan kovalen nonpolar, pasangan elektron ikatannya akan sama kuat ke semua atom, di mana keelektronegatifan antar ikatannya sama. Contohnya adalah atom H yang berikatan dengan atom H lagi, keduanya memiliki nilai keelektronegatifan masing-masing 2,1. Contoh lainnya adalah minyak. Nah, itu dia jenis-jenis ikatan kovalen.

Pengertian Senyawa Polar Dan Non Polaruy PDF
Perbedaan yang jelas dari mereka, pelarut polar dan nonpolar merupakan pelarut polar melarutkan senyawa polar, sedangkan pelarut nonpolar melarutkan senyawa nonpolar. Polaritas suatu senyawa adalah sifat memiliki kutub. Dalam kimia, itu adalah pemisahan muatan dalam molekul yang memiliki atom atau kelompok atom dengan keelektronegatifan berbeda.
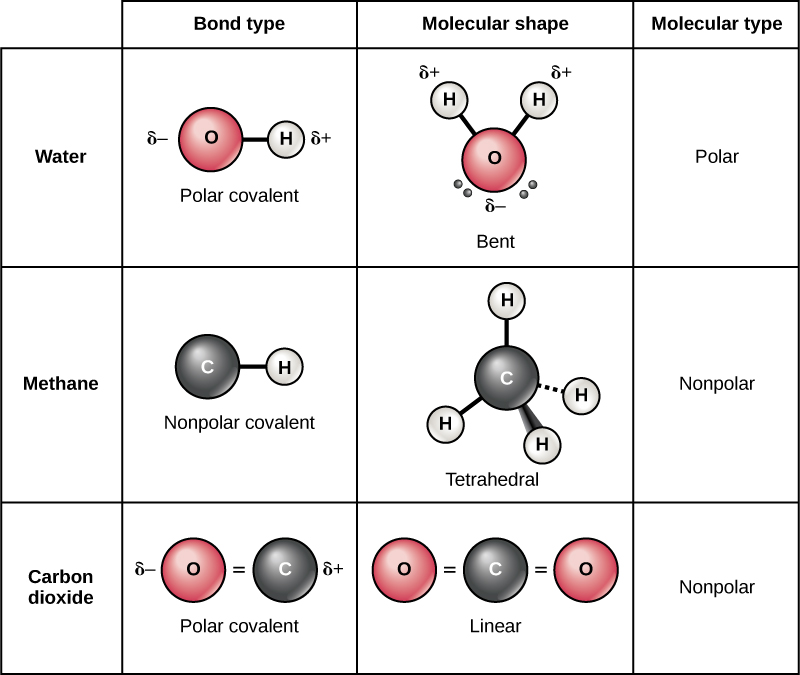
Difference Between Polar and Nonpolar Molecules Definition, Formation, Properties, Examples
Contoh senyawa non polar antara lain gas mulia seperti helium (He), neon (Ne), dan argon (Ar), serta senyawa organik seperti hidrokarbon, metana (CH4), etana (C2H6), dan propana (C3H8). Jenis senyawa ini juga dapat terbentuk dari ikatan antara atom-atom yang sama, seperti molekul O2, N2, dan H2. Karena atom-atom tersebut memiliki.

Pelarut Polar dan Nonpolar dalam IPA, pengertian, perbedaan
Pengertian Senyawa Non Polar. Dilansir dari Encyclopedia Britannica, senyawa non polar adalah senyawa yang tidak memiliki muatan listrik bersih (muatan negatif dan positifnya sama sehingga saling menghilangkan) dan memiliki susunan yang simetris. Artinya, enyawa non polar disebut simetris karena semua sisi atom pusatnya terikat pada elemen dan.

Ikatan Kovalen NonPolar vs Polar Perbedaan dan Perbandingan
Molekul nonpolar juga terbentuk ketika atom berbagi ikatan polar mengatur sedemikian rupa sehingga muatan listrik membatalkan satu sama lain. Contoh molekul nonpolar meliputi: Salah satu gas mulia: He, Ne, Ar, Kr, Xe (Ini adalah atom, bukan molekul secara teknis.) Salah satu elemen diatomik homonuklear: H 2 , N 2 , O 2 , Cl 2 (Ini benar-benar.

🔴IKATAN KOVALEN POLAR & NON POLAR, 🔴SENYAWA KOVALEN POLAR DAN SENYAWA KOVALEN NONPOLAR YouTube
Senyawa kovalen non polar juga biasanya memiliki bentuk gas atau cair pada suhu kamar. Baca juga: Ikatan Kovalen Koordinasi: Pengertian dan Contohnya. Ikatan kovalen non polar terjadi karena kesamaan keelektronegativan atom-atom yang saling terikat. Di mana jika perbedaan keelektronegativan dua atom di bawah 0,4.
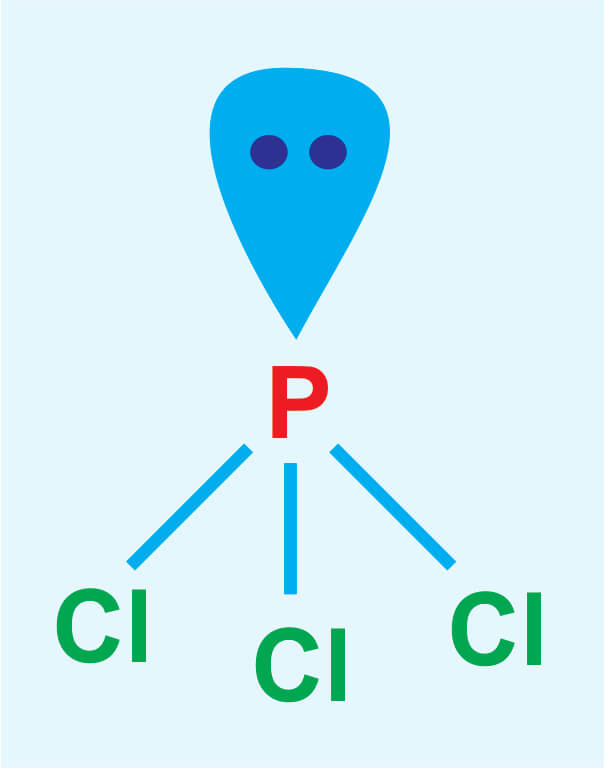
Pengertian senyawa polar dan nonpolar 2021
Dilansir dari Sciencing, senyawa polar memiliki beberapa sifat, yaitu: Senyawa polar memiliki muatan positif dan negatif parsial. Saat berikatan, atom dapat saling berbagi electron atau kovalen atau melepaskan elektron atau ionik. Perbedaan anatar molekul polar dan nonpolar ditentukan oleh vektor muatan parsial yang dihasilkan dari setiap ikatan.
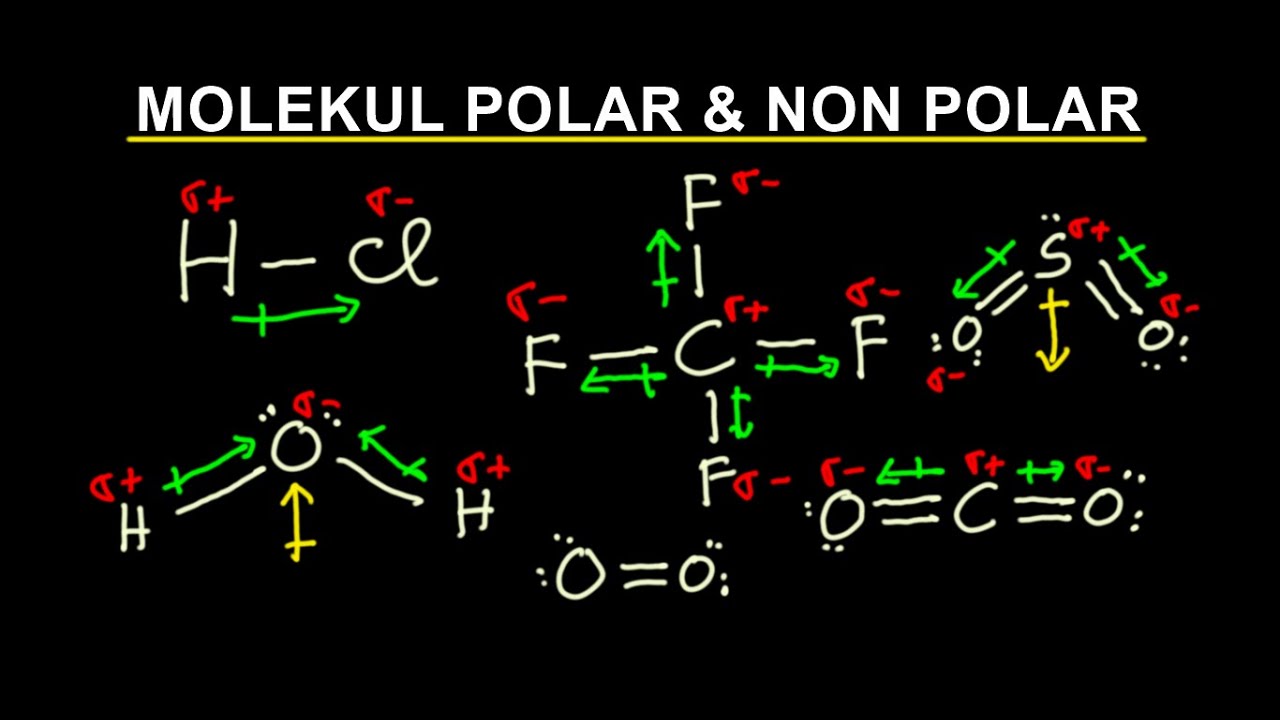
MOLEKUL POLAR & NON POLAR YouTube
Dalam pengertian singkat, non polar merupakan jenis yang dapat terbentuk karena adanya suatu ikatan antara elektron pada unsur-unsur yang membentuknya. Hal tersebut bisa terjadi karena unsur yang berikatan memiliki nilai elektronegativitas yang sama atau hampir sama. Baca Juga: Senyawa yang Memiliki Ikatan Hidrogen, Jenis, dan Kegunaannya.