
Hidrolisis Garam Pengertian, Macam, Dan Rumus, Beserta Contoh Soalnya Secara Lengkap
Asam + basa → garam + air. HCl + KOH → KCl + H2O. Garam dapur (NaCl) diperoleh dari air laut yang mengalami penguapan dan kristalisasi. Untuk menjadikannya garam beryodium, harus diproses iodisasi (garam kalium/KI). Sifat-sifat atau ciri-ciri garam: Larut dalam air. Contohnya : KNO3, NH4Cl, Na2SO4. Sukar larut dalam air.

Pengertian Asam, Basa, Garam, Ciri, Sifat, Indikator & Contoh
4. Rumus tetapan hidrolisis garam yang berasal dari asam lemah dan basa lemah. Karena hidrolisis garam yang berasal dari asam lemah dan basa lemah dapat terhidrolisis sempurna, alias bisa bersifat asam, basa, maupun netral. Maka rumus tetapan hidrolisis garamnya adalah sebagai berikut: BH + (aq) + H 2 O (l ) → B (aq) + H 3 O + (aq)

20+ Contoh Soal Hidrolisis Asam Lemah Dan Basa Kuat Contoh Soal Terbaru
pH larutan garam yang berasal dari asam lemah dan basa lemah sebesar 26,67%. Data hasil wawancara yang dilakukan terhadap beberapa siswa yang mengalami miskonsepsi dijelaskan penyebab miskonsepsi yang terjadi. Berdasarkan hasil penelitian dapat disimpilkan bahwa miskonsepsi yang terjadi di kelas XI MIA 3

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 21
Oleh karena itu garam dapat terbentuk dari 4 reaksi hidrolisis kimia sebagai berikut: Garam yang berasal dari asam lemah dan basa kuat bersifat netral dan memiliki pH = 7, yang artinya tidak terjadi hidrolisis. Garam dari asam kuat dan basa lemah, di mana garam ini akan memiliki pH < 7 alias bersifat asam. Garam dari asam lemah dan basa kuat.

Perhitungan pH Garam dari Asam lemah dan Basa Lemah
Dalam bahasa Yunani, hidrolisis berasal dari kata hidro yang berarti air dan lisis yang berarti. Garam Parsial (Asam Lemah-Basa Kuat) Hidrolisis parsial terjadi ketika suatu garam yang terbentuk dari reaksi asam basa dimana asam lemah dan basa kuat dilarukan di dalam air, maka yang terjadi yaitu kation dari basa tidak dapat terhidrolisis.

Pengertian asam basa dan garam berserta contohnya PR Sekolahku
Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya. Misalnya garam yang terbentuk dari asam kuat dan basa kuat, garam yang terbentuk dari asam kuat dan basa lemah, garam yang terbentuk dari asam lemah.
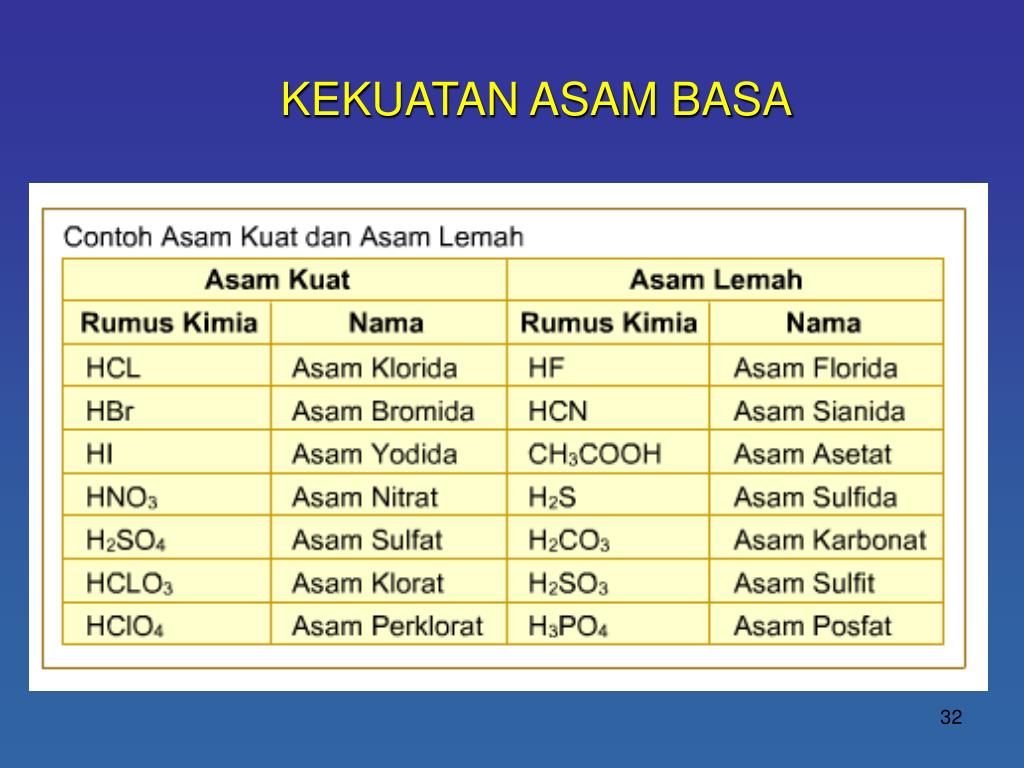
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
3. Garam dari basa kuat dan asam lemah, garam ini bersifat basa (pH >7). Contoh: 4. Garam dari asam lemah dan basa lemah, sifat asam/basa bergantung pada nilai Ka dan Kb dari senyawa tersebut. Contoh: Pengertian Hidrolisis. Photo by Timo Volz on Unsplash. Hidrolisis berasal dari kata hydro yang berarti air dan lysis yang berarti peruraian.

Larutan garam yang berasal dari asam lemah dan basa lemah...
Berdasarkan asam basa pembentuknyagaram dibedakan menjadi empat, yaitu. 1. Garam dari asam kuat dan basa kuat. Larutan garam yang berasal dari asam kuat dan basa kuat ini bersifat netral atau tidak terhidrolisis dalam air. Larutannya memiliki pH = 7, seperti NaCl dan K 2 SO 4. 2. Garam dari asam lemah dan basa kuat.

Rangkuman Materi Asam, Basa, Garam
3. Garam yang terbentuk dari komponen asam lemah dan basa lemah. Garam yang berasal dari asam lemah dan basa lemah dalam air akan mengalami hidrolisis total, karena kedua komponen garam (anion asam lemah dan kation basa lemah) terhidrolisis akan menghasilkan ion H + dan ion OH -, sehingga pH larutan ini bergantung pada nilai K a dan K b. Rumus :

PPT BAB 2 ASAM, BASA DAN GARAM PowerPoint Presentation, free download ID5075424
Garam yang berasal dari asam lemah dan basa lemah mengalami hidrolisis sempurna. Garam ini terionisasi dalam air menghasilkan ion-ion. Kation dan Anion keduanya berasal dari asam lemah dan basa lemah. Kedua ion tersebut mengalami hidrolisis sempurna. Garam yang termasuk jenis ini antara lain:CH 3 COONH 4, (NH 4) 2 CO 3.
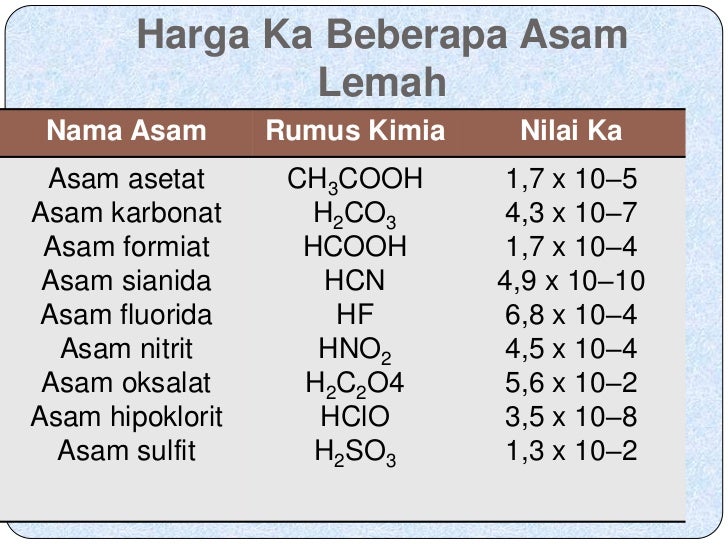
Nama Asam Dan Basa Beserta Rumus Kimianya
BaF2 merupakan senyawa garam yang berasal dari asam kuat HBr dan basa lemah NH4OH sehingga sifat hidrolisisnya adalah hidrolisis sebagian dan memiliki sifat asam atau pH < 7. CaSO4 adalah senyawa garam yang terbentuk dari asam kuat H2SO4 dan basa kuat Ca(OH)2 sehingga akan bersifat netral dan tidak mengalami reaksi hidrolisis garam.

27+ Contoh Soal Hidrolisis Asam Lemah Basa Lemah Contoh Soal Terbaru
Jika harga K a. . = K b. . , berarti [H+] = [OH−], sehingga garam bersifat netral. Dengan demikian, larutan garam yang berasal dari asam lemah dan basa lemah akan bersifat basa jika K a < K b. Baca pembahasan lengkapnya dengan daftar atau masuk akun Ruangguru. GRATIS!

Hidrolisis Garam Pengertian, Macam, Rumus, Dan Contoh Soal
Pembahasan : Hidrolisis yang berasal dari asam lemah dan basa lemah merupakan hidrolisis total, sebab kedua ion garam mengalami reaksi hidrolisis dengan air. Dari soal diatas penyusun dari garam NH 4 CN adalah NH 4 OH ( basa lemah ) dan HCN ( asam lemah ) Dan akan terjadi hidrolisis total. Maka NH 4 CN akan terionisasi menjadi NH 4+ dan CN - .
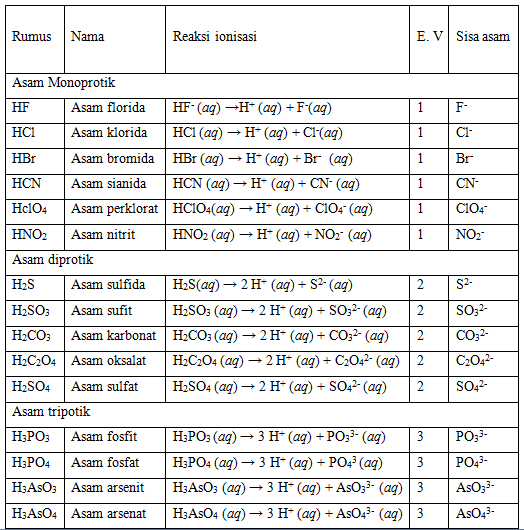
Teori Asam Basa dan Garam Siswapedia
yang berasal dari basa lemah dan anion yang berasal dari asam lemah dapat mengalami hidrolisis garam. Kekuatan asam basa telah dijelaskan pada teori asam basa Bronsted Lowry. Pada teori asam basa Bronsted Lowry telah dijelaskan tentang hubungan asam basa konjugasi. Sesuai dengan pernyataan Mujiwati (2014), bahwa konsep kekuatan asam basa dan.

Hidrolisis Garam dari Asam lemah dan Basa Kuat Rumus Kimia
Asam dan basa dapat bereaksi menghasilkan air serta senyawa ionic garam. Reaksi itu disebut reaksi netralisasi. Asam dan basa merupakan dua jenis larutan yang kerap digunakan dalam kehidupan sehari-hari manusia. Asam dan basa ada yang memiliki sifat kuat dan juga lemah. Berikut daftar nama asam kuat, asam lemah, basa kuat, dan juga basa lemah:

Mengenal Asam Basa Sifat, Cara Membedakan, dan Klasifikasinya Kimia Kelas 11
2. Garam yang Berasal dari Basa Lemah dan Asam Kuat. Garam seperti NH 4 Cl yang dapat terbentuk dari reaksi asam kuat (HCl) dan basa lemah (NH 3) akan mengalami hidrolisis kation yang berasal dari basa lemah sehingga larutannya bersifat asam.Anion Cl − tidak terhidrolisis karena merupakan basa konjugasi yang sangat lemah.. Kation NH 4 + dapat terhidrolisis karena merupakan asam konjugasi.