
Hidrolisis Garam Soal dan Pembahasan KIMIA KELAS 11 YouTube
Rumus Hidrolisis Garam. 1. Garam yang terbentuk dari komponen asam lemah dan basa kuat. Garam yang berasal dari asam lemah dan basa kuat dalam air akan mengalami hidrolisis sebagian. Komponen garam (anion asam lemah) mengalami hidrolisis menghasilkan sebuah ion OH -, maka pH > 7 sehingga larutan garam bersifat basa.

PERCOBAAN HIDROLISIS GARAM; MENENTUKAN SIFAT DAN pH LARUTAN GARAM YouTube
Hasil pengembangan bahan ajar kimia materi hidrolisis garam tervalidasi secara empirik oleh ahli isi dan ahli materi pembelajaran kimia dinilai valid dengan skor rata-rata 3,67 dan layak digunakan.

Konsep Reaksi Hidrolisis Garam Materi Hidrolisis Garam Kimia SMA Kelas 11 YouTube
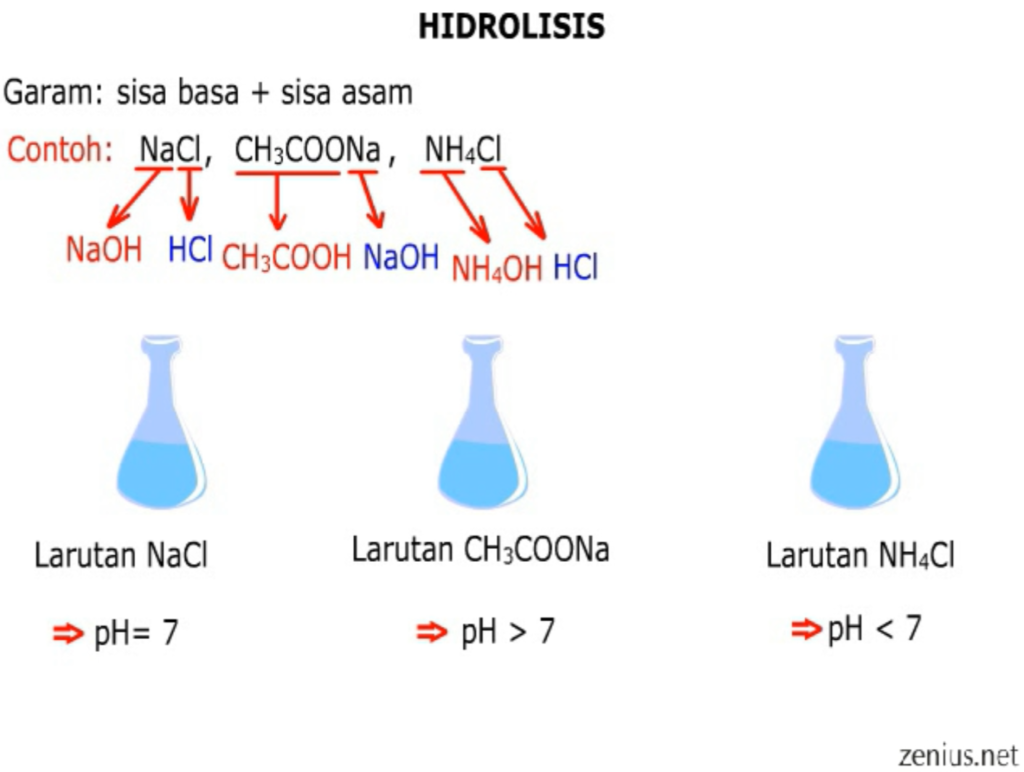
Hidrolisis Garam . Nah setelah mengetahui mengenai "garam" itu sendiri, sekarang mari kita perhatikan gambar di atas yang menunjukkan berbagai jenis larutan garam dengan pH yang berbeda, pertanyaannya kenapa bisa berbeda? Hal ini terjadi akibat adanya hidrolisis.

PPT Hidrolisis Garam PowerPoint Presentation, free download ID2077463
Garam yang terbentuk dari proses netralisasi antara asam kuat dan basa lemah akan bersifat asam. Contohnya NH4Cl, FeCL₃, CuCl₂, AlCl₃, CuSO₄, dan lain-lain. Begini persamaannya: NH 4 Cl (aq) = Cl - (aq) + NH 4+ (aq) Ion amonium yang terbentuk mengalami hidrolisis garam untuk membentuk amonium hidroksida dan ion H⁺.

Hidrolisis Adalalah Manfaat Fungsi Rumus Jenis Mekanisme Reaksi The Best Porn Website
Hidrolisis Garam. Hidrolisis Garam - Pengantar. Ketika suatu asam bereaksi dengan suatu basa maka akan dihasilkan senyawa ionik yang disebut garam. Larutan garam dapat bersifat netral, asam, ataupun basa. Hal ini dikarenakan terjadinya hidrolisis garam, yaitu reaksi dari suatu kation atau suatu anion, ataupun keduanya, dengan air menghasilkan.

Hidrolisis Garam dari Asam lemah dan Basa Kuat Rumus Kimia
Halo, video ini adalah animasi materi kimia hidrolisis garam (SMA Kelas 11) yang ditujukan untuk penilaian akhir mata kuliah Micro Teaching.Dosen Pengampu: L.

Teori Hidrolisis Garam 1 YouTube
Sifat Hidrolisis Garam. Hidrolisis garam merupakan reaksi reversible penguraian garam oleh air. Reaksi ini bekerja pada salah satu ion-ion garam (kation atau anion) dengan air sehingga membentuk larutan bersifat asam atau basa. Sifat asam atau basa yang dihasilkan pun bergantung pada jenis asam basa yang membentuk garam tersebut.

Hidrolisis Garam Kimia Kelas 11 YouTube
Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya. Misalnya garam yang terbentuk dari asam kuat dan basa kuat, garam yang terbentuk dari asam kuat dan basa lemah, garam yang terbentuk dari asam lemah.

Contoh Soal Hidrolisis Garam Dan Pembahasannya Foto Modis
1. Hidrolisis parsial. Hidrolisis parsial ialah ketika garam direaksikan dengan air hanya salah satu/sebagian ion saja yang mengalami reaksi hidrolisis, sedangkan yang lainnya tidak. Komponen penyusun garam yang mengalami reaksi hidrolisi parsial ini ialah asam lemah dan basa kuat atau sebaliknya. 2. Hidrolisis total.

Hidrolisis Garam Kimia Kelas 11 • Part 5 Contoh Soal Perhitungan pH Larutan Garam (2) YouTube
Manfaat Hidrolisis Garam dalam Kehidupan. Proses hidrolisis garam memiliki banyak manfaat dalam kehidupan sehari-hari. Contohnya adalah: Garam amonium nitral (NH 4 NO 3) yang merupakan campuran dari basa lemah dan asam kuat. Sehingga garam ini bersifat asam. Amonium nitrat biasanya digunakan untuk alat kompres dingin.

Hidrolisis Garam Pengertian, CiriCiri Dan Sifat Sifat Larutan Garam Pelajaran Sekolah Online
Manfaat Reaksi Hidrolisis. Reaksi hidrolisis ini banyak diterapkan dalam kehidupan sehari hari, berikut ini beberapa contoh manfaat dari hidrolisis dalam kehidupan: Hidrolisis berperan dalam pembentukan garam dapur (NaCl) yang merupakan reaksi antara basa kuat dengan asam kuat. Garam dapur ini banyak digunakan sebagai bahan penyedap dalam makanan.

Hidrolisis Garam YouTube
Ion aqua mengalami hidrolisis, pada tingkat yang lebih besar atau lebih kecil. Langkah hidrolisis pertama diberikan secara umum sebagai: M (H 2 O) nm+ + H 2 O ⇌ M (H 2 O) n − 1 (OH) (m − 1) + + H 3 O +. Dengan demikian kation air bertindak sebagai asam dalam hal teori asam basa Brønsted-Lowry.

Terbaru Rumus Hidrolisis Garam Baru
3. Garam yang terbentuk dari komponen asam lemah dan basa lemah. Garam yang berasal dari asam lemah dan basa lemah dalam air mengalami hidrolisis total, karena kedua komponen garam (anion asam lemah dan kation basa lemah) terhidrolisis menghasilkan ion H + dan ion OH-, sehingga harga pH larutan ini tergantung harga Ka dan Kb.. Contoh: NH4CN, (NH4)2S, CH3COONH4, dan sebagainya.

Hidrolisis Garam
Ion Na + berasal dari basa kuat (NaOH), sedangkan ion Cl - berasal dari asam kuat (HCl), karena perbandingan H + dan OH - sama, maka tidak akan terhidrolisis dan garam bersifat netral.. 2. Hidrolisis garam asam kuat dengan basa lemah dapat terhidrolisis dan bersifat asam. Hidrolisis garam asam kuat dengan basa lemah dapat terhidrolisis, namun hanya terhidrolisis parsial. Karena jika.
Hidrolisis Garam Materi Kimia Kelas 11
Hidrolisis garam merupakan reaksi antara air dengan ion-ion yang berasal dari asam lemah atau basa lemah dari suatu garam. Komponen garam (kation atau anion) berasal dari asam lemah dan basa lemah membentuk ion H 3 3 O + + dan OH − −. Sebagaimana kita ketahui bahwa jika larutan asam direaksikan dengan larutan basa akan membentuk senyawa garam.

Garam yang Mengalami Hidrolisis dan Sesuai Hasil Reaksinya YouTube
Rumus pH Larutan Garam. Contoh Soal Hidrolisis Garam. Contoh Soal #1: Contoh Soal #2: Jika makanan terasa hambar, tentunya Sobat Pijar akan menambahkan garam agar rasanya menjadi asin. Salah satu senyawa garam paling umum adalah NaCl atau biasa dikenal dengan garam dapur yang biasa Sobat Pijar konsumsi sehari-hari itu.